أعلن باحثون في اليابان عن تطوير تقنية نانوية فريدة لتوصيل الأجسام المضادة العلاجية مباشرة إلى المستضدات (Antigens) داخل الخلايا السرطانية، في خطوة تمثل تقدمًا مهمًا نحو تحسين فعالية العلاج الموجه للسرطان. نُشرت نتائج الدراسة في Journal of Controlled Releaseبتاريخ 4 يونيو 2025.
باستخدام شبكة معدنية–بوليفينولية (Metal–Polyphenol Network, MPN)، استطاع النظام اجتياز الحويصلات الداخلية (Endosomes) داخل الخلية، مما أتاح الاستهداف الخلوي المباشر للأجسام المضادة. ونتج عن ذلك تثبيط نمو الأورام وزيادة النشاط المضاد للسرطان، مما يجعل هذه التقنية أداة واعدة في العلاج الموجه.
تجاوز الحواجز الخلوية: نواقل نانوية قائمة على البوليفينولات لتوصيل الأجسام المضادة
ينتج الجهاز المناعي بروتينات على شكل حرف “Y” تُعرف بالأجسام المضادة (Antibodies) للتعرف على المواد الغازية وتحييدها. وعند التعرف على مؤشرات محددة أو مستضدات على سطح الورم، تستهدف الأجسام المضادة العلاجية — وهي بروتينات مصممة اعتمادًا على الأجسام المضادة الطبيعية — الخلايا السرطانية مع حماية الأنسجة السليمة، ما يعزز قدرة الجهاز المناعي على مقاومة السرطان.
ورغم أن الأجسام المضادة العلاجية أثبتت فعاليتها في استهداف سطح الخلية، إلا أن قدرتها داخل الخلية محدودة بسبب عدم قدرتها على عبور الأغشية الخلوية وتفادي الاحتجاز داخل الحويصلات الداخلية — وهي حجرات غشائية صغيرة تحتجز الجزيئات داخل الخلية. ولتجاوز هذه العقبة، يجري البحث في تقنيات مختلفة تمنع احتجاز الأجسام المضادة داخل الحويصلات الداخلية.
التقنية اليابانية المبتكرة
فريق بحثي من مختبر الكيمياء وعلوم الحياة في معهد العلوم بطوكيو (Science Tokyo)، بقيادة الأستاذ المساعد يوتو هوندا والبروفيسور نوبوهيرو نيشياما، نجح في معالجة هذه المشكلة باستخدام البوليفينولات — وهي مركبات طبيعية توجد في النبيذ والنباتات — لتصميم “آلة نانوية” مبتكرة محملة بالأجسام المضادة.
شارك مركز الابتكار في الطب النانوي التابع لمعهد كاواساكي للترويج الصناعي في تطوير هذه التقنية.
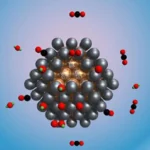
توضح الدراسة ابتكار ناقل نانوي بوليمري يعتمد على شبكة معدنية–بوليفينولية (MPN) لإيصال الأجسام المضادة العلاجية مباشرة إلى داخل الخلايا السرطانية. تعتمد الاستراتيجية على قدرة البوليفينولات على تمكين الأجسام المضادة من الإفلات من الحويصلات الداخلية وتوزيعها داخل الخلية.
خطوات التطوير
بدأ الباحثون بدمج حمض التانيك (Tannic Acid, TA) — وهو أحد البوليفينولات — مع بولي إيثيلين جلايكول (PEG) لتكوين مركب PEG–TA، وهو نظام حامل نانوي يتميز بثبات عالٍ وخصائص إخفاء مناعية (Stealth Properties).
لتحضير مركب MPN محمّل بالأجسام المضادة، جرى مزج جزيئات PEG–TA مع الجسم المضاد العلاجي وأيونات كلوريد الحديد الثلاثي (Fe³⁺). وتم تحليل خصائص هذه الآلات النانوية باستخدام المجهر الإلكتروني النافذ (TEM) وتقنية مطابقة الارتباط الفلوري (FCS)، حيث بلغ قطرها 30 نانومتر — وهو حجم مثالي للتطبيقات الطبية الحيوية.
الاختبارات والنتائج
- في المختبر (In vitro): قيست كفاءة الامتصاص الخلوي وإيصال الأجسام المضادة.
- في الجسم الحي (In vivo): تم اختبار النشاط المضاد للأورام في نموذج فأر يحمل سرطان ثدي مقاوم للعلاج.
أظهرت النتائج أن هذه النواقل النانوية مستقرة للغاية في الدورة الدموية، مع امتصاص متزايد من قبل الخلايا السرطانية، مما أدى إلى خفض نمو الورم بنسبة 20% مقارنة بمجموعة التحكم غير المعالجة. وقد عُزي التأثير المضاد للأورام إلى آلية إطلاق الأجسام المضادة المبتكرة.
آلية الإفلات من الحويصلات الداخلية
عند دخول هذه النواقل النانوية إلى الخلية السرطانية، يتم احتجازها مبدئيًا داخل الحويصلات الداخلية. وبسبب الحموضة الداخلية (pH منخفض)، تنفصل شبكة MPN عن الأجسام المضادة، وتحدث تأثيرًا معادلاً (Buffering Effect) يشجع دخول البروتونات والأيونات المقابلة من خارج الحويصلة.
يتسبب ذلك في إضعاف غشاء الحويصلة الداخلية ورفع الضغط الأسموزي الداخلي، مما يؤدي إلى تمزق الحويصلة وإطلاق الأجسام المضادة داخل السيتوبلازم، حيث يمكنها الارتباط بالمستضدات الداخلية.
أثر علاجي مباشر
كشفت الدراسة عن توصيل ناجح لجسم مضاد موجه ضد بروتين S100A4، ما أدى إلى استعادة وظيفة بروتين p53 الكابح للأورام، وبالتالي تحفيز موت الخلايا السرطانية. كما أظهرت النتائج سمية منخفضة، مما يدعم أمان هذه التقنية.
خاتمة الباحثين
صرّح هوندا: “دراستنا تمثل خطوة مهمة نحو تطوير جيل جديد من العلاجات الخلوية المعتمدة على الأجسام المضادة. إن التصميم غير الكاتيوني، المتوافق حيويًا، والقابل للحقن الجهازي لنظامنا القائم على MPN يمكن أن يوسّع تطبيقاته لتتجاوز السرطان، مما يمهد الطريق نحو استهداف دوائي من الجيل القادم”
مرجع الدراسة:
Honda, Y., وآخرون (2025). “نواقل نانوية بوليمرية قائمة على الشبكات المعدنية–البوليفينولية لتسهيل توصيل الأجسام المضادة إلى السيتوبلازم وتحقيق تأثيرات مضادة للأورام في نماذج سرطان الثدي”. Journal of Controlled Release. DOI: 10.1016/j.jconrel.2025.113929
المصدر:
معهد العلوم بطوكيو
* مراجعة: لورا طومسون: تخرّجت لورا طومسون من جامعة مانشستر متروبوليتان حاصلةً على درجة البكالوريوس في اللغة الإنجليزية وعلم الاجتماع. وخلال دراستها، عملت لورا كمدققة لغوية، ثم واصلت العمل في هذا المجال بدوام كامل قبل أن تنتقل لاحقًا للعمل كمحررة مواقع إلكترونية في شركة رائدة في مجال التحليلات والإعلام.