خلاصة البحث
تكشف دراسة جديدة أن شكل الألياف النانوية (Nanofibers)، وليس تركيبها الكيميائي وحده، يلعب دورًا جوهريًا في إحداث سمّية الرئة. فقد أظهرت النتائج أدلة على مستوى البروتين قد تساعد في تصميم مواد نانوية أكثر أمانًا وذكاءً. نُشرت الدراسة في مجلة Nano Today، مؤكدة أن مورفولوجيا الألياف — بما في ذلك الطول والقطر والصلابة — تتحكم بشكل حاسم في كيفية استجابة الخلايا الرئوية للتعرض.
تحول هذه الدراسة الحديث عن السموم النانوية من التركيب الكيميائي إلى البنية، لكن هذه الدراسة تنقل الحوار نحو البنية الشكلية (Morphology). فقد بيّنت أن الشكل وحده قادر على تحفيز الالتهاب وإحداث تلف خلوي.
مورفولوجيا الألياف النانوية
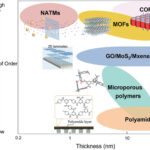
الألياف النانوية تُستخدم على نطاق واسع في تخزين الطاقة، تنقية المياه، التطبيقات الطبية وغيرها. لكن شكلها الرقيق والممدود يثير مخاطر عند استنشاقها. ووفق منظمة الصحة العالمية، تُعتبر “الألياف الخطرة” التي قطرها أقل من 3 ميكرون، وطولها أكبر من 5 ميكرون، ونسبة الطول إلى العرض تتجاوز 3:1، لأن هذه الألياف ترتبط بأمراض مثل تليّف الرئة والأورام المتوسطة “الميزوثليوما”.
نموذج ألياف المسبب للمرض (Fiber Pathogenicity Paradigm) يربط بين المتانة والشكل والسمّية، لكن عاملًا مهمًا غالبًا ما يُغفل وهو الصلابة. تُشكّل هذه الصلابة مشكلةً عندما تواجه الخلايا البلعمية في الرئتين أليافًا طويلةً وصلبة؛ إذ لا تستطيع ابتلاعها بالكامل. تُؤدي فشل الاستجابة المناعية، المعروفة باسم البلعمة المُحبطة (Frustrated Phagocytosis)، إلى التهابٍ مُستمر. ، والتي تفضي إلى التهاب مزمن.
تتعمق الدراسة الجديدة في تفاصيل هذا الصراع الخلوي، بهدف ابتكار أدوات للتنبؤ بالسمّية تعتمد على النماذج الخلوية، متجاوزة الحاجة إلى التجارب الحيوانية.
فصل الشكل عن التركيب
لاختبار تأثير المورفولوجيا بمعزل عن التركيب الكيميائي، استخدم الباحثون ألياف كربيد السيليكون (SiC) وثاني أكسيد التيتانيوم (TiO₂) في شكلهما الأصلي والمطحون ميكانيكيًا. الألياف الأصلية كانت أطول وأكثر صلابة. بعد الطحن، أصبحت أقصر وأقل سمّية، إذ تمكنت الخلايا من ابتلاعها بسهولة أكبر.
عرّض الباحثون خلايا البلعمية السنخية في الجرذان (NR8383) لكل نوع من الألياف، واستخدموا اختبارات خلوية متقدمة مع تقنية الكروماتوغرافيا السائلة المقترنة بقياس الطيف الكتلي (LC-MS/MS) لتتبع الاستجابات.
وقد شملت الاختبارات قياس مؤشرات الإجهاد الخلوي الأساسية:
- إنزيم لاكتات ديهيدروجيناز (LDH) كمؤشر على تلف الغشاء الخلوي،
- بيروكسيد الهيدروجين كمؤشر على الإجهاد التأكسدي،
- إنزيم بيتا-غلوكورونيداز كمؤشر على تسرب الجسيمات الحالة،
- وبروتين عامل نخر الورم-ألفا (TNF-α) كمؤشر على الالتهاب.
أكدت صور المجهر الإلكتروني الماسح (SEM) أن الألياف السليمة من كربيد السيليكون (SiC) بلغ متوسط طولها 9.5 ميكرون وقطرها 156 نانومتر، بينما كانت ألياف ثاني أكسيد التيتانيوم (TiO₂) أقصر وأنحف. وقد أدى الطحن الميكانيكي إلى تقليل طول الألياف بشكل كبير، مما سمح بابتلاعها الكامل داخل الخلايا وتسبّب بآثار سمّية أقل.
البصمة البروتينية للسمّية
أثبتت النتائج أن المورفولوجيا كان لها أثر مباشر في السمية حيث أن الألياف الأصلية سببت ثقب الأغشية الخلوية، والبلعمة المحبطة، وارتفاع الإشارات الالتهابية. بينما الألياف المطحونة تم ابتلاعها بسهولة أكبر وأحدثت تأثيرات أقل حتى عند التركيزات العالية.
كشف التحليل البروتيومي أن:
- التعرض لألياف SiC غير المطحونة غيّر مستويات أكثر من 1000 بروتين بعد 18 ساعة.
- الألياف المطحونة غيّرت 10 بروتينات فقط.
- ألياف TiO₂ غير المطحونة غيّرت 266 بروتينًا، مقابل 5 فقط عند طحنها.
وأكّد تحليل المكوّنات الرئيسية (PCA) أن العينات المطحونة تجمّعت معًا، مما يدعم أن الشكل هو العامل الحاسم.
كما لوحظت زيادة في بروتينات مرتبطة بالالتهاب مثل أرجيناز-1 (Arginase-1) ومضاد مستقبل الإنترلوكين-1 (IL-1RA).
بينما ارتفع ميثيونين سلفوكسيد (Methionine Sulfoxide) كمؤشر للإجهاد التأكسدي، خاصة في الخلايا المعرضة لـ SiC.
أما بروتينات الليسوسومات (Lysosomal Proteins) فقد وُجدت في الوسط المحيط بالخلايا بدلًا من داخلها، ما يؤكد حدوث تمزق ليسوسومي. وكانت مؤشرات النخر (Necrosis) أكثر ظهورا من تلك المرتبطة بالموت الخلوي المبرمج (Apoptosis).
بصمة عالمية لسمّية النانو
بناءً على هذه النتائج، اقترح الفريق البحثي لوحة من 58 بروتينًا كـ “بصمة سُمّية قائمة على المورفولوجيا”.
تشمل هذه اللوحة مسارات مرتبطة بالالتهاب، سلامة الليسوسومات، الأيض، والموت الخلوي. والأهم أن هذه البصمة مستقلة عن نوع المادة، مما يعني إمكانية استخدامها للتنبؤ بالسمية عبر أنواع مختلفة من الألياف النانوية.
هذا له أهمية كبيرة، إذ يمكن للباحثين الاعتماد على اختبارات مخبرية in vitro مدعومة بهذه البصمة البروتينية لفحص المواد النانوية مبكرًا في مرحلة التصميم، بدلًا من الاعتماد الكلي على التجارب الحيوانية. وهو ما يتماشى مع مبدأ 3R (الاستبدال، التقليل، التحسين) في علم السموم، ويدعم التوجّه التنظيمي والصناعي نحو بدائل أخلاقية ومستدامة.
نحو نانوتكنولوجيا أكثر أمانًا
يقدم هذا البحث رؤية جديدة حول سلامة الألياف النانوية. ومع تزايد وجودها في السلع الاستهلاكية، التطبيقات الصناعية، وحتى الطب، يصبح فهم تفاعلاتها البيولوجية أمرًا أكثر إلحاحًا.
من خلال التركيز على الاستجابات على مستوى البروتينات، توضح الدراسة الآليات الكامنة وراء سمّية الألياف النانوية، وتفتح الطريق أمام هندسة مواد أكثر أمانًا، وأطر تنظيمية أكثر دقة.
ويؤكد الباحثون على ضرورة التحقق المستقبلي من هذه البصمة البروتينية باستخدام خلايا بشرية أولية، ودراسات تحاكي التعرض المزمن طويل الأمد، مع توسيع نطاق التجربة ليشمل مواد نانوية ونماذج حيوية أخرى، بهدف تعزيز قوة التنبؤ ودقة التقييم.
الهوامش:
المرجع البحثي: Stobernack, T., et al. (2025). Predicting the morphology-driven pathogenicity of nanofibers through proteomic profiling. Nano Today, 65, 102812. DOI: 10.1016/j.nantod.2025.102812
رابط الدراسة: https://www.sciencedirect.com/science/article/pii/S1748013225001847
الكاتب محمد أسامة: استشاري بيانات ومحلل مستقل من دلهي، الهند. حاصل على بكالوريوس في الهندسة الميكانيكية مع تخصص في الذكاء الاصطناعي والروبوتات من جامعة Galgotias بالهند. لديه خبرة واسعة في كتابة المحتوى التقني، علم البيانات والتحليلات، والذكاء الاصطناعي.
الترجمة: بمساعدة منصات الذكاء الاصطناعي